Multiphase Equilibrium
多相平衡の数理:エネルギー最小化からラッチフォード・ライスの式へ
Rachford-Rice Equation (Flash Calculation)
Variable: $\psi$ (Vapor Fraction)
1. 序論:自然は「安定」を目指す
コップに入った水が蒸発して空気と混ざり合うとき、あるいは密閉容器の中で気体と液体が共存するとき、そこには目に見えない厳密なルールが存在します。それが「多相平衡(Multiphase Equilibrium)」です。
自然界のあらゆるシステムは、放置すれば必ず「最も居心地の良い状態」、すなわちエネルギーが最も低い状態へと遷移します。この「安定点」を見つけ出すことこそが、化学プラントの設計から新素材の開発に至るまで、工学における最大のテーマの一つです。
本稿では、熱力学の基本原理である「エネルギー最小化」から出発し、ラグランジュの未定乗数法を経て、最終的に化学工学の基本式である「ラッチフォード・ライスの式」が導かれる過程を概観します。
2. 熱力学的アプローチ:ギブスエネルギーの定義
平衡状態において最小化されるべき指標、それが「ギブスの自由エネルギー ($G$)」です。
多成分系において、全ギブス自由エネルギー $G_{total}$ は、各成分の「化学ポテンシャル($\mu$)」と「物質量($n$)」の総和として表されます。
ここで、化学ポテンシャル $\mu_i$ は、以下のように対数項(エントロピー項)を含んだ形で定義されます。
\[ \mu_i = \mu_i^\circ + RT \ln \frac{n_i}{N} \]この式の対数項($RT \ln \dots$)はエントロピーに由来します。「濃度が低い(希薄な)ほど、ポテンシャルは低くなる($-\infty$ に近づく)」という性質を表しており、物質が「濃い場所」から「薄い場所」へ拡散しようとする駆動力の根源です。
3. ラグランジュの未定乗数法による導出
単に $G$ を小さくすれば良いわけではありません。密閉系では「各成分の総物質量は変わらない」という制約条件(Mass Balance)が存在します。
「制約付きの最小化問題」を解くための最強のツールが、ラグランジュの未定乗数法です。
気液2相系において、ある成分 $i$ の総モル数 $N_i$ は一定です。
\[ g_i(n) = n_{i, Gas} + n_{i, Liq} - N_i = 0 \]目的関数 $G_{total}$ から、制約条件 $g_i$ に未定乗数 $\lambda_i$ を掛けたものを引いて、ラグランジュ関数 $\mathcal{L}$ を作ります。
\[ \mathcal{L} = \sum_{i} (n_{i, G} \mu_{i, G} + n_{i, L} \mu_{i, L}) - \sum_{i} \lambda_i (n_{i, G} + n_{i, L} - N_i) \]安定点(極値)では、各変数の偏微分が $0$ になります。例えば、気相の物質量 $n_{i, G}$ で偏微分すると、
\[ \frac{\partial \mathcal{L}}{\partial n_{i, G}} = \mu_{i, G} - \lambda_i = 0 \quad \Rightarrow \quad \mu_{i, G} = \lambda_i \]同様に、液相についても $\mu_{i, L} = \lambda_i$ となります。
この結果、未定乗数 $\lambda_i$ を介して以下の重要な結論が数学的に導かれます。
この物理的条件を出発点として、実用的な気液平衡定数 $y_i = K_i x_i$ が定義されます。
4. ラッチフォード・ライスの式
上記の平衡条件と物質収支式を組み合わせ、変数として「気化率 $\psi$(システム全体の何割が気体になったか)」を導入して整理したものが、ラッチフォード・ライスの式です。
\[ \sum_{i=1}^N \frac{z_i (K_i - 1)}{1 + \psi (K_i - 1)} = 0 \]この方程式の解 $\psi$ を求めることが、フラッシュ計算(気液平衡計算)のゴールとなります。
5. 解析条件と定数設定
今回は、具体的な数値解を求めるため、以下のモデルと定数を用いてシミュレーションを行いました。
使用したモデル:ラウールの法則
平衡定数 $K_i$ は温度 $T$ と圧力 $P$ の関数ですが、今回は理想系を仮定し、アントワン式(Antoine Equation)による蒸気圧を用いた以下のモデルを採用しました。
\[ K_i(T) = \frac{P_i^{sat}(T)}{P_{sys}}, \quad \log_{10} P_i^{sat} = A_i - \frac{B_i}{T + C_i} \]($P_{sys}$: 全圧, $P_i^{sat}$: 純成分の蒸気圧)
シミュレーション条件
- 対象系: メタン(C1) / エタン(C2) / プロパン(C3) の3成分系
- 全圧 ($P_{sys}$): 20.265 bar
原料組成 ($z_i$) と アントワン定数 ($A, B, C$):
| 成分 | 組成 $z_i$ | A | B | C |
|---|---|---|---|---|
| Methane (C1) | 0.20 | 4.22 | 516.68 | 11.19 |
| Ethane (C2) | 0.30 | 4.50 | 663.70 | -16.64 |
| Propane (C3) | 0.50 | 4.53 | 803.81 | -24.79 |
(Antoine定数は bar, K 単位系換算値を使用)
6. 解析結果
上記の定数を代入したラッチフォード・ライスの式を、擬似過渡解析を用いて解いた結果を示します。
横軸に温度 $T$、縦軸に気化率 $\psi$ をとり、全液相状態から全気相状態への相転移を追跡しました。
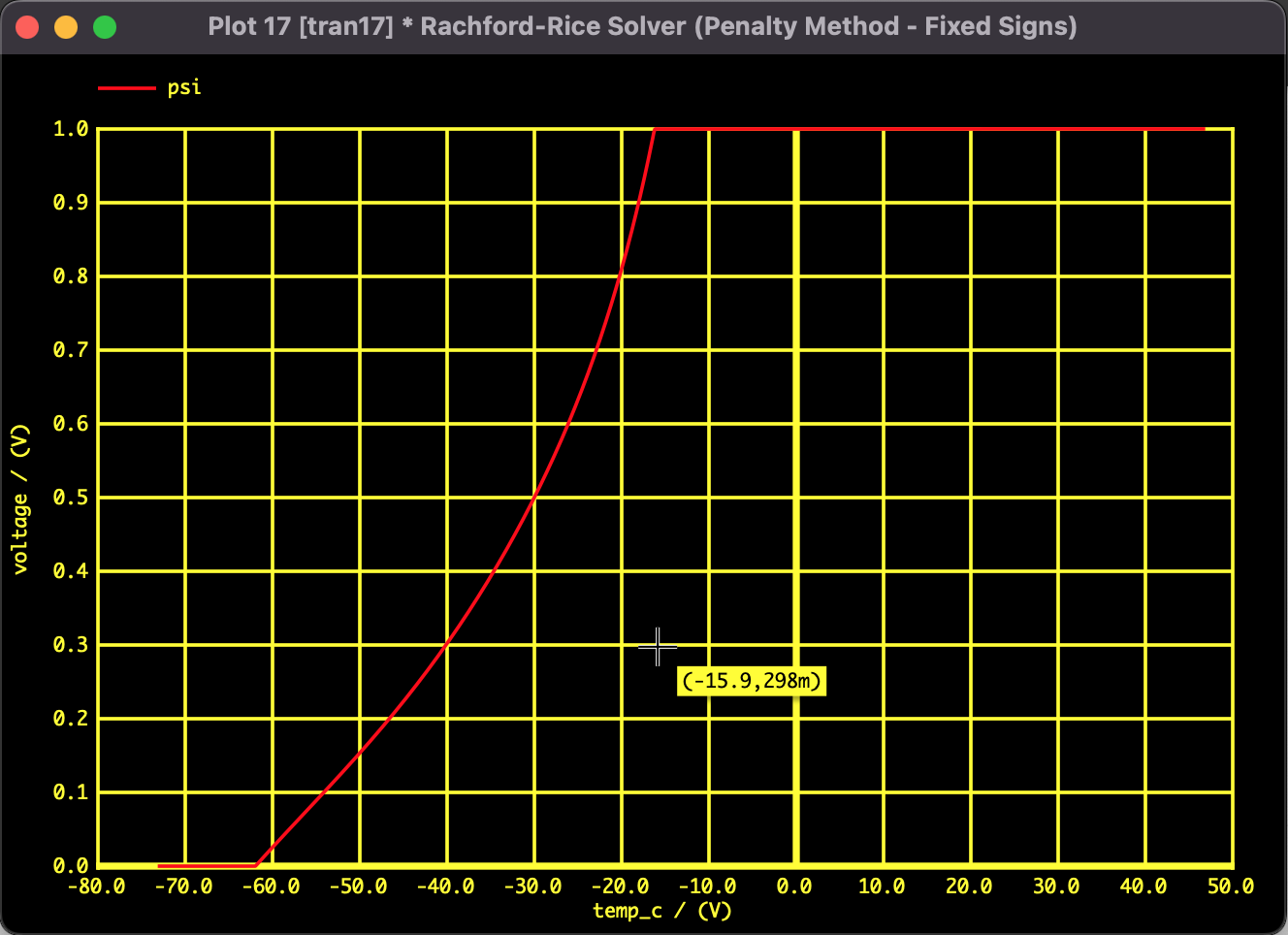
- -61.2℃付近: $\psi=0$ から立ち上がり、沸騰が開始(Bubble Point)。
- -61.2℃ 〜 -15.6℃: 3成分が揮発度の違いにより徐々に気化していく遷移領域。
- -15.6℃付近: $\psi=1$ に到達し、全ての液体が蒸発(Dew Point)。
ペナルティ関数を組み込んだ擬似過渡解析を用いることで、方程式の解が物理的な定義域($0 \le \psi \le 1$)内に留まり、かつ急激な相変化の領域でも計算が発散することなく、S字を描くような連続的な解曲線を得ることができました。
解析環境
- SPICE: Mac SPICE3
- PC: MacBook
- OS: macOS Monterey 12.7.6
- CPU: 1.2GHz デュアルコア Intel Core m5
- メモリ: 8GB
この規模の計算では現在のPC環境であれば一瞬で収束するため、詳細な計算時間の計測は割愛いたします。